
臨床成績
国内第Ⅰ/Ⅱ相臨床試験継続調査(JR-031-202試験)3)
3)社内資料:同種造血幹細胞移植後に発症した標準治療抵抗性の急性移植片対宿主病(急性GVHD)に対するJR-031投与の第Ⅰ/Ⅱ相試験
(JR-031-201)及び継続調査(JR-031-202)(承認時評価資料)
1. 24ヵ月後までの生存率
先行試験(JR-031-201)に引き続き本試験を開始した11例の患者のうち、9ヵ月後までに2例の死亡が確認され、24ヵ月後の時点で生存していた患者は9例(64.3%、両側95%信頼区間:35.1〜87.2)でした。なお、本試験の終了直後に患者1例の死亡が確認されています。
24ヵ月後までの生存率
| 初回投与時の GVHDグレード |
グレードⅡ (n=9) |
グレードⅢ (n=5) |
全体 (n=14) |
|||
|---|---|---|---|---|---|---|
| 生存者数 | 例数 | 例数 | 例数 | 割合(%) | 両側95%信頼区間 | |
| JR-031-201試験 | 12週後 | 8 | 4 | 12 | 85.7 | 57.2〜98.2 |
| 100日後 | 7 | 4 | 11 | 78.6 | 49.2〜95.3 | |
| 24週後 | 7 | 4 | 11 | 78.6 | 49.2〜95.3 | |
| JR-031-202試験 | 24ヵ月 | 6 | 3 | 9 | 64.3 | 35.1〜87.2 |
24ヵ月後までの生存曲線
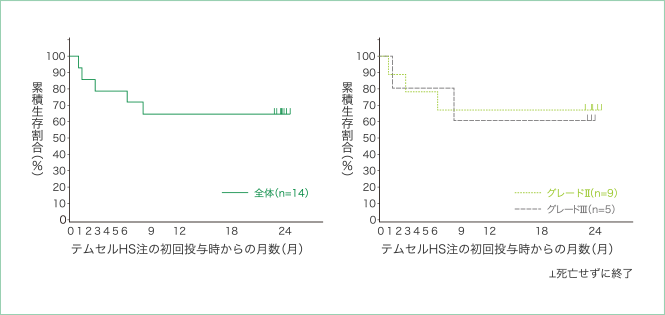
本試験の開始時である24週後から12ヵ月後までの約6ヵ月間に副作用を発現した患者は、11例中1例(1件)で、再発急性骨髄性白血病が認められました。また、12ヵ月後の時点で本試験に参加していた9例のうち、12ヵ月後から24ヵ月後までに副作用を発現した患者はいませんでした。
24週後から24ヵ月後までに死亡に至った副作用は、再発急性骨髄性白血病1件でした。
- 注:本試験では、12ヵ月後以降に発現した有害事象については、治験責任医師により重篤及び重要な有害事象又は本品との因果関係が否定できない有害事象に限って収集したため、本試験の開始時(先行試験の24週後)から12ヵ月後までに発現した有害事象と12ヵ月後から24ヵ月後までに収集した有害事象については2つの時期に分けて集計を行った
JCRファーマ株式会社
Copyright2016, JCR Pharmaceuticals Co., Ltd. All Rights Reserved.



















