
臨床成績
国内第Ⅱ/Ⅲ相臨床試験(JR-031-301試験)4)
4)社内資料:同種造血幹細胞移植後に発症したステロイド抵抗性の急性移植片対宿主病(急性GVHD)に対するJR-031投与の第Ⅱ/Ⅲ相試験
(JR-031-301)(承認時評価資料)
1. 28日間以上継続するCR(主要評価項目)
初回投与時から24週後までの期間に28日間以上継続するCRが認められた患者は、25例中12例(48.0%、両側95%信頼区間:27.8〜68.7)でした。
28日間以上継続するCR
| CR継続日数※1 | 例数※2( n=25) | 割合(%) | 両側95%信頼区間 |
|---|---|---|---|
| 28日間以上 | 12 | 48 | 27.8〜68.7 |
- ※1:GVHDが再燃した場合:CR継続日数(日)=(GVHD再燃の発現日)−(直前のCR発現日)
CRのまま終了した場合:CR継続日数(日)=(24週後内で最終のGVHD評価日)−(直前のCR発現日)+1 - ※2:本品投与後に二次治療が行われた患者を除く
2. 各時点における治療効果判定(副次評価項目)
初回投与時から4週後の時点においてORと判断された患者は、25例中15例(60.0%、両側95%信頼区間:38.7〜78.9)であり、信頼区間の下限が有効性を示すうえで最低限上回るべき割合(35%)を超えていました。
初回投与時から12週後及び24週後の時点においてORと判断された患者の割合の推移を確認したところ、いずれの時点も4週後の時点の評価に比べて、CRと評価された患者数の増加が認められました。
初回投与4週後、12週後及び24週後の時点の治療効果判定
| 時期 | 4週後 | 12週後 | 24週後 | ||||||
|---|---|---|---|---|---|---|---|---|---|
| 治療効果判定 | 例数 (n=25) |
割合 (%) |
両側95% 信頼区間 |
例数 (n=25) |
割合 (%) |
両側95% 信頼区間 |
例数 (n=25) |
割合 (%) |
両側95% 信頼区間 |
| 全反応:OR | 15 | 60.0 | 38.7〜 78.9 |
11 | 44.0 | 24.4〜 65.1 |
10 | 40.0 | 21.1〜 61.3 |
| 完全反応:CR | 6 | 24.0 | 9.4〜 45.1 |
11 | 44.0 | 24.4〜 65.1 |
9 | 36.0 | 18.0〜 57.5 |
| 部分反応:PR | 9 | 36.0 | 18.0〜 57.5 |
0 | 0.0 | 0.0〜 13.7 |
1 | 4.0 | 0.1〜 20.4 |
| 混合反応:MR | 4 | 16.0 | 4.5〜 36.1 |
0 | 0.0 | 0.0〜 13.7 |
0 | 0.0 | 0.0〜 13.7 |
| 悪化:PG | 0 | 0.0 | 0.0〜 13.7 |
0 | 0.0 | 0.0〜 13.7 |
0 | 0.0 | 0.0〜 13.7 |
| 変化なし:NC | 1 | 4.0 | 0.1〜 20.4 |
0 | 0.0 | 0.0〜 13.7 |
0 | 0.0 | 0.0〜 13.7 |
| 死亡又は評価不能 | 5 | 20.0 | 6.8〜 40.7 |
14 | 56.0 | 34.9〜 75.6 |
15 | 60.0 | 38.7〜 78.9 |
- 本品投与後に二次治療が行われた場合は、二次治療の実施日以降の評価を無効とした
3. 52週後までの生存率(副次評価項目)
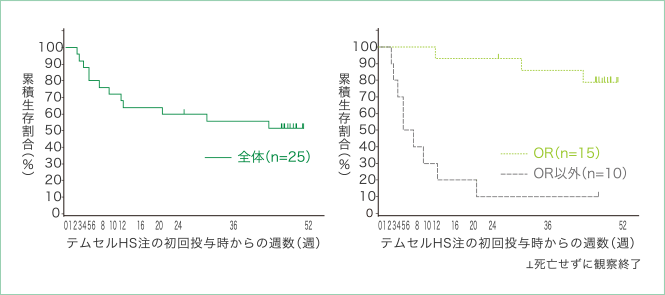
本品の投与を開始した25例の患者のうち、4週後までに3例、100日後までに6例、24週後までに1例の死亡が確認され、24週後の評価時点で生存していた患者は15例(60.0%、両側95%信頼区間:38.7〜78.9)でした。その後、180日後から52週後までの期間に2例の死亡が確認され、52週後の評価時点で生存が確認された患者は13例(52.0%、両側95%信頼区間:31.3〜72.2)でした。
初回投与時から4週後の時点のGVHD評価別に集計を行ったところ、4週後の時点のGVHD評価がORであった患者15例のうち、52週後の評価時点で生存が確認された患者は12例(80.0%、両側95%信頼区間:51.9〜95.7)でした。一方で、4週後の時点のGVHD評価がOR以外であった患者10例のうち、52週後の評価時点で生存が確認された患者は1例(10.0%、両側95%信頼区間:0.3〜44.5)でした。
- ※180日後、52週後の例数には生存に関する情報のない患者1例を含む
52週後までの生存率
| 初回投与4週後 の時点の評価 |
OR(CR又はPR)(n=15) | OR以外(n=10) | 全体(n=25) | ||||||
|---|---|---|---|---|---|---|---|---|---|
| 生存者数 | 例数 | 割合 (%) |
両側95% 信頼区間 |
例数 | 割合 (%) |
両側95% 信頼区間 |
例数 | 割合 (%) |
両側95% 信頼区間 |
| 4週後 | 15 | 100.0 | 78.2〜 100.0 |
7 | 70.0 | 34.8〜 93.3 |
22 | 88.0 | 68.8〜 97.5 |
| 100日後 | 14 | 93.3 | 68.1〜 99.8 |
2 | 20.0 | 2.5〜 55.6 |
16 | 64.0 | 42.5〜 82.0 |
| 24週後 | 14 | 93.3 | 68.1〜 99.8 |
1 | 10.0 | 0.3〜 44.5 |
15 | 60.0 | 38.7〜 78.9 |
| 180日後 | 14 | 93.3 | 68.1〜 99.8 |
1 | 10.0 | 0.3〜 44.5 |
15 | 60.0 | 38.7〜 78.9 |
| 52週後 | 12 | 80.0 | 51.9〜 95.7 |
1 | 10.0 | 0.3〜 44.5 |
13 | 52.0 | 31.3〜 72.2 |
- 180日後、52週後の例数には生存に関する情報のない患者1例を含む
52週後までの生存曲線
4. 副腎皮質ステロイド剤の投与量(副次評価項目)
本品初回投与時の副腎皮質ステロイド剤の一日投与量の平均値は71.38mgと最も多く、4週後の時点で 45.15mg、8週後の時点で31.00mgまで減少していることを確認しました。
副腎皮質ステロイド剤の一日投与量※1,※2の分布
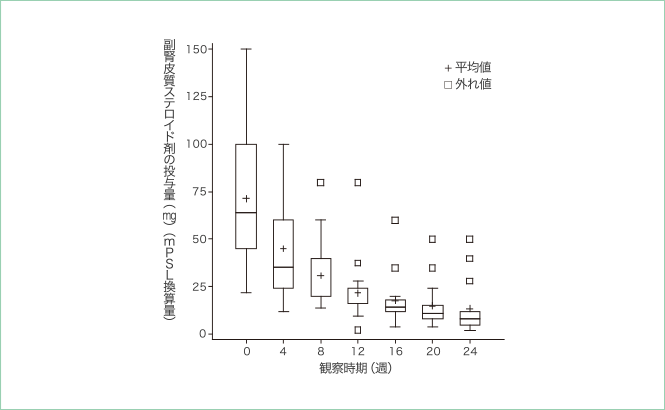
- ※1:当該観察時期のGVHD評価日に使用された副腎皮質ステロイド剤の投与量
- ※2:mPSL換算量(PSLを使用していた場合には1.25で除した)
5. CRに至るまでの期間(副次評価項目)
本品の本投与(8回)の投与期間に該当する27日までの期間にCRに至った患者は累積すると25例中8例(32.0%)であり、続く28〜55日の期間にCRに至った患者は25例中6例(24.0%)でした。初回投与時からCRに至るまでの期間については、患者による差はあるものの、初回投与時から8週後(56日)にかけて徐々にCRに至っていることが確認されました。
CRに至るまでの期間
| CRに至るまでの期間※1 | CRに至った例数 | 割合(%) |
|---|---|---|
| 0日〜6日 | 1 | 4.0 |
| 7日〜13日 | 2 | 8.0 |
| 14日〜20日 | 4 | 16.0 |
| 21日〜27日 | 1 | 4.0 |
| 28日〜55日 | 6 | 24.0 |
| 56日以上 | 0 | 0.0 |
- n=25
- ※1:初回投与時からCRに至るまでの期間(日)=(最初のCR発現日)−(初回投与日)
本品投与後に二次治療が行われた場合は、二次治療の実施日以降の評価を無効とした
CRに至るまでの期間のKaplan-Meier曲線
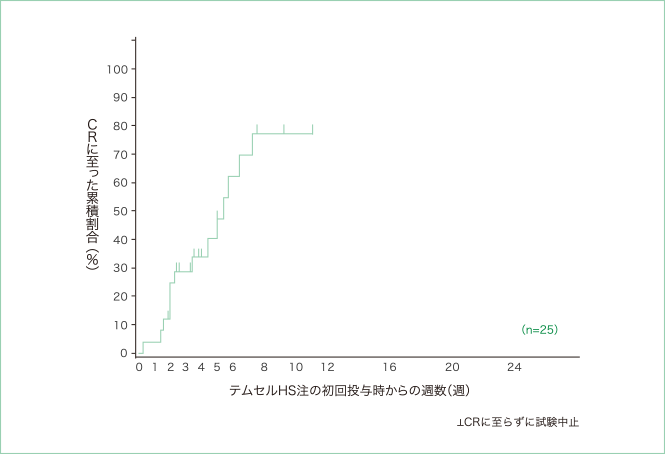
- 本品投与後に二次治療が行われた場合は、二次治療の実施日以降の評価を無効とした
6. 各臓器別の治療効果判定(副次評価項目)
24週後までに一度でも臓器障害が消失したと判断された患者は、皮膚の症状を有した患者が12例中8例(66.7%、両側95%信頼区間:34.9〜90.1)、肝臓の症状を有した患者が11例中4例(36.4%、両側95%信頼区間:10.9〜69.2)、消化管の症状を有した患者が20例中16例(80.0%、両側95%信頼区間:56.3〜94.3)でした。
各臓器別の最大治療効果判定
| 臓器 | 皮膚(n=12)※1 | 肝臓(n=11)※1 | 消化管(n=20)※1 | ||||||
|---|---|---|---|---|---|---|---|---|---|
| 期間 | 例数※2 | 割合 (%) |
両側 95% 信頼区間 |
例数※2 | 割合 (%) |
両側 95% 信頼区間 |
例数※2 | 割合 (%) |
両側 95% 信頼区間 |
| 4週後 | 5 | 41.7 | 15.2〜 72.3 |
3 | 27.3 | 6.0〜 61.0 |
14 | 70.0 | 45.7〜 88.1 |
| 12週後 | 8 | 66.7 | 34.9〜 90.1 |
4 | 36.4 | 10.9〜 69.2 |
16 | 80.0 | 56.3〜 94.3 |
| 24週後 | 8 | 66.7 | 34.9〜 90.1 |
4 | 36.4 | 10.9〜 69.2 |
16 | 80.0 | 56.3〜 94.3 |
- ※1:臓器ごとのステージが初回投与時からの期間においてすべて「0」の場合は含めない
- ※2:治療効果判定において、期間中に一度でもCR(臓器障害の消失)と判断された患者
本品投与後に二次治療が行われた場合は、二次治療の実施日以降の評価を無効とした
JCRファーマ株式会社
Copyright2016, JCR Pharmaceuticals Co., Ltd. All Rights Reserved.


















